人が本来持つ組織修復能力を最大限に引き出す“再生誘導医薬”の開発に注力―株式会社ステムリム 代表取締役社長COO 岡島 正恒
株式会社ステムリム
証券コード 4599/東証マザーズ
代表取締役社長COO 岡島 正恒
Masatsune Okajima

iPS細胞をはじめとする再生医療とは異なるアプローチで難病治療に取り組んでいる領域の一つが“再生誘導医薬”。研究・開発は大阪大学との共同で進行しており、治験の段階まで来た。再生誘導医薬を開発するステムリムの岡島正恒社長に今後の見通しを聞いた。
取材・文/山本 信幸 写真撮影/和田 佳久
細胞を培養する再生医療とは異なるアプローチで取り組む
―― 「再生誘導医薬」という事業について教えてください。
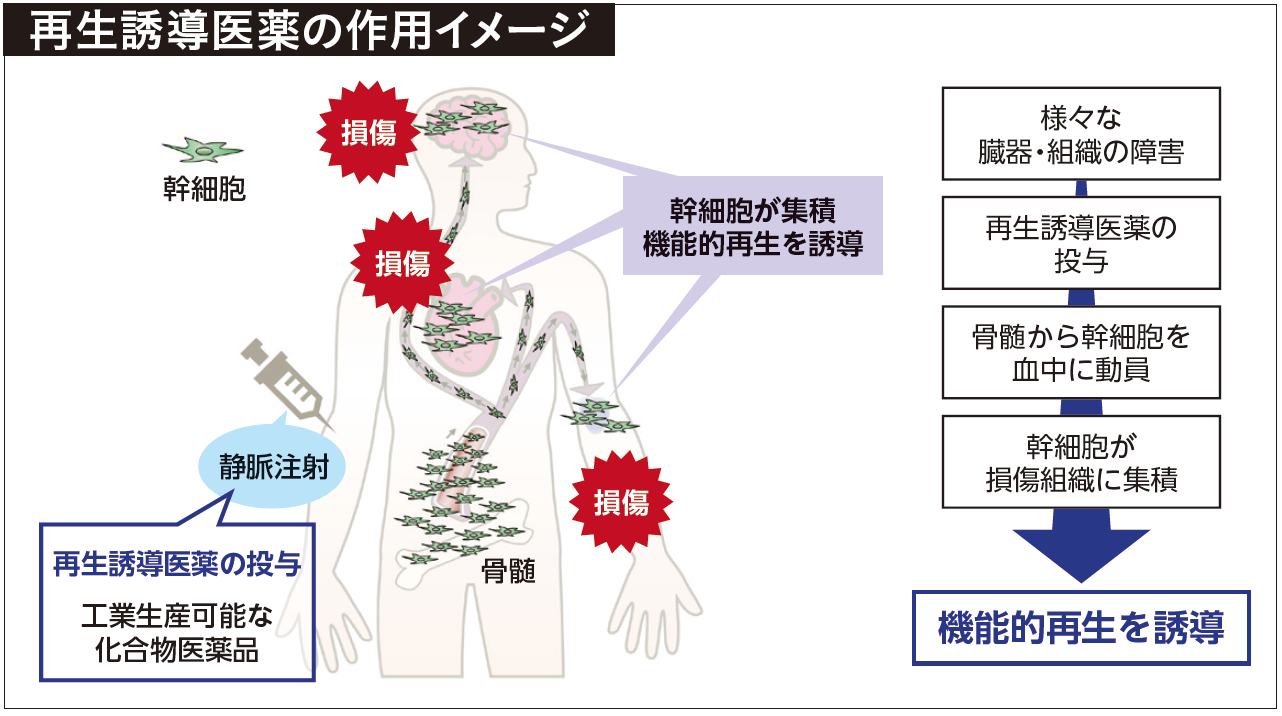
岡島 当社の創業以来、研究開発に取り組んできた「再生誘導医薬」は、文字通り体の再生を誘導する医薬品です。
具体的には、患者さんの静脈から再生誘導医薬を投与することで、骨髄から細胞の修復を促す幹細胞(間葉系幹細胞)を血液に引き出し、損傷した組織に集めて再生を誘導します。幹細胞は神経や皮膚、骨、軟骨、筋肉、血管などの組織に分化する能力を持っているので、脳梗塞や脊髄損傷などの中枢神経系疾患、心筋梗塞や心筋症のような循環器系疾患、難治性皮膚潰瘍などの上皮系疾患といった組織損傷をともなう数多くの難病に対して幅広い治療効果を副作用なくもたらすことが期待できます。
―― iPS細胞やES細胞を使った再生医療とは違うものなのですか。
岡島 再生医療は体から取り出した細胞を培養して増やし、もう一度生きた細胞を体内に戻す治療手法です。自分に戻す場合は自家移植、他人に移植する場合は他家移植と呼ばれます。生きた細胞は、品質の管理が難しく、細胞が変質・癌化するなど安全性への懸念があり、治療可能時期の制約や免疫拒絶反応といった課題を抱えています。脳に移植する場合は、頭蓋骨に穴を開けて細胞を投与することになり、患者さんへの肉体的な負担も大きいと言えます。
一方、再生誘導医薬はペプチドやタンパクといった工業生産が可能な化合物医薬品なので、徹底した品質管理と安定した製造が可能です。従来の医薬品と同じく医療機関に常備しておき、必要な時にいつでも投与ができることや、患者さん本人の幹細胞を動員するための化合物医薬品なので免疫拒絶がないことなどさまざまな利点があります。
再生医療の世界市場は2050年には38兆円規模に
―― 創業の目的と研究の進行状況を教えてください。
岡島 当社はコーポレートミッションを「再生誘導で難治性疾患を克服する」と定めており、再生誘導医薬の発明者で大阪大学大学院の玉井克人教授らの研究成果を基にした医薬品の開発を目的として2006年に設立しました。
07年に大阪大学との共同研究を開始し、研究成果の知財化を進めてきました。これまでに日本を始め米国、欧州、中国など世界各国で84件の特許を取得し、グローバル展開を目指しています。
この研究により皮膚の難病である表皮水疱症や、脳梗塞などに適応する再生誘導医薬として「HMGB1ペプチド」を開発し、14年に塩野義製薬とライセンス契約を結んでいます。
―― 国の承認を得るための臨床試験は始まっているのですか。
岡島 17年3月にHMGB1ペプチドに関する表皮水疱症を対象とした医師主導治験(フェーズⅠ=健康な人に使用する段階)が終わり、フェーズⅡ(患者に使用する段階)に移行しています。また19年4月からは脳梗塞を対象とした治験(フェーズⅡ)も始まっています。
――再生医療の市場規模について教えてください。
岡島 経済産業省による再生医療の市場規模予測では、国内の市場規模は2020年に950億円、50年には2兆5,000億円、世界の市場規模ではそれぞれ1兆円と38兆円という大幅な拡大が見込まれています。
なお、「再生誘導医薬」は全世界で当社のみが取り組む新規分野であり、間葉系幹細胞での治療効果が見込めるすべての領域がターゲットになります。
製薬会社から受け取る契約金や使用許諾料が主な収入
―― どのようなビジネスモデルなのでしょうか。
岡島 医薬品の上市(発売)までには、「発見・基礎研究」、「候補同定・薬効確認」、「非臨床試験」、「臨床試験」、「承認申請・製造販売」というステップがあります。当社は発見・基礎研究を行った大阪大学との間で、成果物における共有特許についての独占実施権の許諾を受けており、発見・基礎研究から臨床試験までが担当領域です。主な役割としては候補物質の同定(決定)、作用メカニズムの証明、製造法の確立、動物モデルおよび早期臨床のPoC(試作開発の前段階における検証)の確立までです。臨床試験以降を担当する製薬会社には開発・製造・販売権のライセンスを与え、ライセンスフィー(契約一時金)、開発の進捗に応じたマイルストーン収入、ロイヤルティー(使用許諾料)を受け取ります。
現在、先にお話したHMGB1ペプチドのほかに、複数のプロジェクトが進行しており、非臨床試験の段階に達しています。
―― 医薬品の上市まで一般に10年程度の開発期間がかかると言われています。株主還元についてはどうお考えですか。
岡島 19年7月期の事業収益は1億円で、これはライセンス契約に基づく臨床データ使用料によるものです。営業損失は7億26百万円、当期純損失は7億21百万円となりました。
20年7月期は、事業収益としてはHMGB1ペプチドに関するマイルストーン収入を見込んでおり、4億円を予想しています。一方、HMGB1ペプチドを用いた再生誘導医薬開発プロジェクトの進捗および新規再生誘導医薬候補物質の探索プロジェクトの推進により、研究開発費が増加するため、営業損失10億90百万円、当期純損失11億37百万円を見込んでいます。
まだ配当を検討する段階ではないので、企業価値を高めてキャピタルゲインでお返しすることになると思います。株主の皆様にはぜひ、長期投資のスタンスで応援していただければと思います。











